Oxit axit: Tính chất hóa học và bài tập

Trong hóa học, oxit axit là một khái niệm được đặc biệt quan tâm và thường được hỏi trong các kỳ thi học kỳ và Trung học Phổ thông. Để giúp các bạn hiểu rõ về oxit axit, tính chất và các bài tập có lời giải, chúng tôi sẽ cung cấp thông tin chi tiết dưới đây.
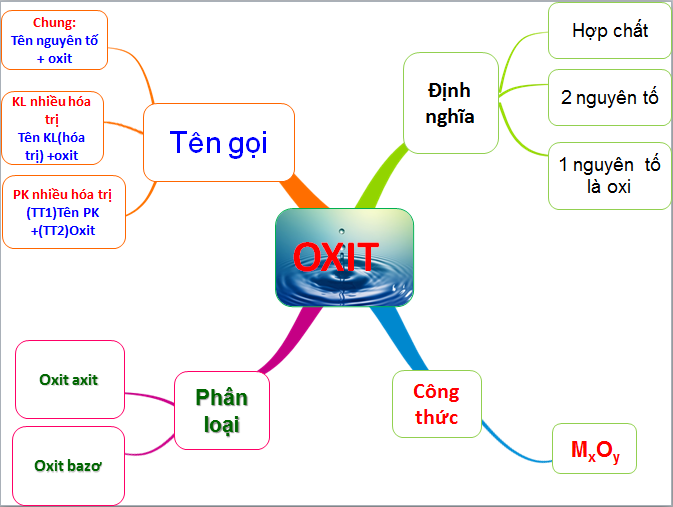
1. Oxit axit là gì?
Oxit axit, hay còn được gọi là anhidrit axit, là một loại oxit có khả năng tác động với bazơ để tạo thành muối hóa học và tác động với nước để tạo thành axit. Thông thường, oxit axit là các hợp chất phi kim và khi tác động với nước sẽ tạo ra các axit tương ứng. Một phân tử oxit axit bao gồm hai nguyên tố hóa học, trong đó một trong số đó là oxi.
2. Cách đặt tên oxit axit
Tên của một oxit axit gồm có các thành phần sau:
- Tên tiền tố chỉ số nguyên tử của phi kim.
- Tên phi kim.
- Tên tiền tố chỉ số nguyên tử của oxi.
- “Oxit”.
Dưới đây là một số ví dụ về cách đọc tên oxit axit:
- ZnO: Kẽm oxit.
- UO2: Urani đioxit.
- SO3: Lưu huỳnh trioxit.
- N2O5: Đinitơ pentaoxit.
- Mn2O7: Đimangan heptaoxit.
3. Phân loại oxit
Oxit có thể được phân loại thành các loại sau:
3.1. Oxit bazơ
Oxit bazơ là những oxit có khả năng tác động với axit để tạo thành muối và nước. Một số oxit bazơ có khả năng tan trong nước và được gọi là kiềm.
Ví dụ: Na2O (thành muối NaOH), Fe2O3 (thành muối Fe(OH)3)…
3.2. Oxit axit
Oxit axit là những oxit có khả năng tác động với bazơ để tạo ra muối và nước, đồng thời phản ứng với nước để tạo ra một axit.
Ví dụ: Mn2O7 (thành axit HMnO4), CO2 (thành axit H2CO3), P2O5 (thành axit H3PO4)…
3.3. Oxit lưỡng tính
Oxit lưỡng tính là loại oxit có khả năng tác động với cả axit và bazơ để tạo muối và nước.
Ví dụ: Al2O3, ZnO.
3.4. Oxit trung tính
Oxit trung tính là loại oxit không phản ứng với nước để tạo bazơ hay axit, cũng không phản ứng với bazơ hay axit để tạo muối.
Ví dụ: CO (cacbon monoxit), NO (nitơ monoxit)…
4. Tính chất hóa học của oxit axit
4.1. Tính chất tan của oxit axit
Hầu hết các oxit axit, trừ SiO2, đều có tính chất tan trong nước để tạo thành dung dịch axit.
Ví dụ:
- SO3 + H2O → H2SO4
- P2O5 + 3H2O → 2H3PO4
- N2O5 + H2O → 2HNO3
- SO2 + H2O → H2SO3
4.2. Tác dụng với nước
Đa số oxit axit tác dụng với nước để tạo thành dung dịch axit, trừ SiO2.
Ví dụ:
- SO3 + H2O → H2SO4
- CO2 + H2O → H2CO3 (phản ứng thuận nghịch)
4.3. Tác dụng với oxit bazo tan để tạo muối
Các oxit thường tác động với nước (Na2O, CaO, K2O, BaO) để tạo muối.
Ví dụ:
- SO3 + CaO → CaSO4
- P2O5 + 3Na2O → 2Na3PO4
4.4. Tác dụng với bazơ tan
Bazo tan là bazo của kim loại kiềm và kiềm thổ mới. Cụ thể, có 4 bazo tan như sau: NaOH, Ca(OH)2, KOH, Ba(OH)2.
Ví dụ:
- P2O5 + 6KOH → 2K3PO4 + 3H2O
- CO2 + Ca(OH)2 → CaCO3
- SiO2 + Ba(OH)2 → BaSiO3
4.5. Oxit lưỡng tính
Oxit lưỡng tính có khả năng tác động với cả axit và bazơ để tạo muối và nước.
Ví dụ: Al2O3, ZnO.
4.6. Oxit trung tính
Oxit trung tính không phản ứng với nước để tạo bazơ hay axit, cũng không phản ứng với bazơ hay axit để tạo muối.
Ví dụ: CO (cacbon monoxit), NO (nitơ monoxit)…
5. Các dạng bài tập oxit axit tác động với bazơ
5.1. Trường hợp 1
Khi các oxit axit (CO2, SO2…) tác động với dung dịch kiềm (KOH, NaOH…), ta có các phương trình hóa học sau:
- CO2 + NaOH → NaHCO3
- CO2 + 2NaOH → Na2CO3 + H2O
Cách giải:
-
Bước 1: Xét tỉ lệ mol giữa bazơ và oxit axit, giả sử là T.
- Nếu T ≤ 1: Sản phẩm thu được là muối axit (phản ứng 1).
- Nếu 1 < T < 2: Sản phẩm thu được là muối axit và muối trung hoà (phản ứng 1 và 2 xảy ra đồng thời).
- Nếu T ≥ 2: Sản phẩm thu được là muối trung hoà (phản ứng 2).
-
Bước 2: Viết phương trình phản ứng và tính toán theo phương trình đó (nếu cả 2 phản ứng xảy ra, cần đặt ẩn và giải hệ phương trình).
-
Bước 3: Tính toán theo yêu cầu của bài tập.
5.2. Trường hợp 2
Khi các oxit axit (CO2, SO2…) tác động với dung dịch kiềm thổ (Ca(OH)2, Ba(OH)2…), ta có các phương trình hóa học sau:
- CO2 + Ca(OH)2 → CaCO3 + H2O
- 2CO2 + Ca(OH)2 → Ca(HCO3)2
Cách giải:
-
Bước 1: Xét tỉ lệ mol giữa bazơ và oxit axit.
- Nếu T ≤ 1: Sản phẩm thu được là muối trung hoà (phản ứng 1).
- Nếu 1 < T < 2: Sản phẩm thu được là muối axit và muối trung hoà (phản ứng 1 và 2 xảy ra đồng thời).
- Nếu T ≥ 2: Sản phẩm thu được là muối axit (phản ứng 2).
-
Bước 2 và bước 3 tương tự trường hợp 1.
6. Bài tập oxit axit có lời giải
Cung cấp dưới đây là một số bài tập oxit axit có lời giải chi tiết.
Bài tập 1:
Tiến hành sục khí CO2 ở điều kiện tiêu chuẩn vào một lượng dư dung dịch Ca(OH)2. Hãy tính khối lượng kết tủa thu được sau phản ứng.
Lời giải:
- Theo đề bài, số mol CO2 = 5,6/22,4 = 0,25 mol
- Ca(OH)2 dư, phản ứng xảy ra theo phương trình:
CO2 + Ca(OH)2 → CaCO3↓ + H2O - Từ phương trình, ta có số mol CaCO3 = 0,25 mol, vậy khối lượng kết tủa là 0,25 x 100 = 25 gam.
Bài tập 2:
Tiến hành dẫn 2,24 lít khí SO2 ở điều kiện tiêu chuẩn vào 150 ml dung dịch NaOH 1 M. Hãy tính nồng độ mol của các chất trong dung dịch sau phản ứng.
Lời giải:
- Theo đề bài, số mol SO2 = 2,24/22,4 = 0,1 mol, số mol NaOH = 1 x 0,15 = 0,15 mol.
- Phản ứng xảy ra theo các phương trình sau:
- SO2 + 2NaOH → Na2SO3 + H2O
- Na2SO3 + H2O → 2NaHSO3
- Từ các phương trình trên, ta tính được số mol NaHSO3 = 0,025 mol và số mol Na2SO3 = 0,075 mol.
- Vậy nồng độ mol của NaHSO3 là 0,025 M và nồng độ mol của Na2SO3 là 0,075 M.
Bài tập 3:
Đốt cháy hoàn toàn 8 gam lưu huỳnh và cho sản phẩm vào dung dịch Ba(OH)2 0,4 M. Sau đó, đun nóng dung dịch được thu được m gam kết tủa. Hãy tính giá trị của m.
Lời giải:
- Theo đề bài, số mol S = 8/32 = 0,25 mol, số mol Ba(OH)2 = 0,4 x 0,5 = 0,2 mol.
- Phản ứng xảy ra theo các phương trình sau:
- S + O2 → SO2
- SO2 + Ba(OH)2 → BaSO3 + H2O
- BaSO3 + H2O → Ba(HSO3)2
- Từ các phương trình trên, ta tính được số mol Ba(HSO3)2 = 0,05 mol.
- Vậy giá trị của m là 0,05 x 106 = 5,3 gam.
Trên đây là những thông tin về oxit axit mà Văn Phòng Tuyển Sinh Y Dược Hà Nội muốn chia sẻ với các bạn. Hy vọng qua bài viết này, bạn đã hiểu rõ về oxit axit là gì, cách đặt tên, tính chất hóa học và cách giải các bài tập oxit axit tác động với bazơ. Nếu bạn còn thắc mắc về oxit axit, đừng ngần ngại liên hệ với chúng tôi bằng cách truy cập vào trang web Văn Phòng Tuyển Sinh Y Dược Hà Nội và nhập thông tin vào hộp thoại hỗ trợ trực tuyến 24/7 để được giải đáp tốt nhất.